| 分享到: | 更多 |
解开埃博拉病毒感染的密码
本报记者 佘惠敏

高福院士(坐姿者)与研究团队成员在实验室讨论实验结果。本报记者 佘惠敏摄
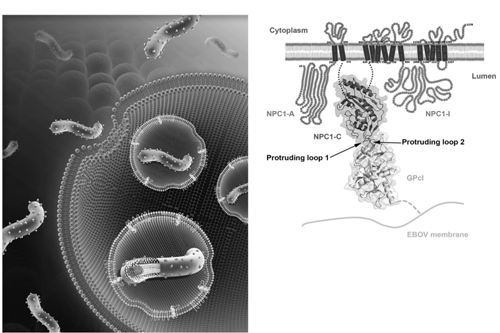
左图 埃博拉病毒入侵模式图 埃博拉病毒为丝状病毒,它入侵宿主细胞时主要有吸附和内吞进入2个步骤。右图 病毒与受体相互作用图 此为在内吞体中,病毒表面糖蛋白与内吞体膜上的NPC1受体结合的分子模式图。 (高福课题组供图)
1月15日,中国科学院院士高福完成了他2004年归国后在生物医学类五大顶级学术期刊发布成果的“大满贯”目标。
这一天,国际权威学术期刊《细胞》发表了中科院微生物研究所高福团队的文章,从分子水平阐释了埃博拉病毒的膜融合激发机制,该机制与此前病毒学家们熟知的四种病毒膜融合激发机制都大为不同,成为第五种病毒膜融合激发机制,这是近年来国际病毒学领域的重大突破。
目前埃博拉治疗没有特异性药物,只有辅助药物。而新机制的发现为抗埃博拉病毒的药物设计提供了新靶点,让我们可能设计出治疗埃博拉的特异性药物。
高福团队如何解开埃博拉病毒感染的密码?
做“表面文章”的实验室
埃博拉,被认为是人类历史上最致命的病毒,自1976年在埃博拉河地区被首次发现后,已在非洲时隐时现,所到之处哀鸿遍野,足足肆虐了近40年。2014年,埃博拉病毒更是首次走出非洲大陆,传播到北美、西欧和南亚,引发了世界性恐慌。那次疫情共导致2.8万多人感染,死亡人数达1.1万多人。
那年9月,高福作为首批援塞医疗队的负责人之一,奔赴疫情严重的塞拉利昂,帮助西非国家从源头上防控埃博拉病毒。工作期间,他在《科学》杂志上发表了题为《行走在塞拉利昂大地上》的现场工作纪实文章,后又在《自然》杂志上发表关于埃博拉病毒基因进化的重大研究成果。
这是高福第一次深入埃博拉病毒疫区,但他对埃博拉病毒的研究,从2011年就已经开始。
接受《经济日报》记者采访时,高福开玩笑说,自己开了一个专做“表面文章”的实验室。
在动物细胞表面,有一层细胞膜,它是生命的防线,阻挡病毒的进入。但细胞膜上也有“带路党”,它们被称作受体,是细胞表面的蛋白质分子。聪明的病毒会利用细胞表面分子的包裹,给自己穿上“迷彩服”,突入细胞防线并增殖产生新的病毒蛋白。被病毒感染的细胞,向上报告“我被感染了,请向我开炮”,生物体就会派出“警察部队”,也就是免疫细胞,来消灭被感染细胞。
要弄清楚病毒是怎么进入细胞里的,就要深入研究细胞的表面——这就是高福实验室做的“表面文章”。高福解释说,“病毒和细胞之间、免疫细胞和被感染细胞之间的界面上到底发生了哪些相互作用,它们是如何互相识别的,又是怎样进行‘对话’的,就是我们正在探索的问题”。
研究表面文章,自然需要有“表面”,所以高福研究的对象是囊膜病毒。病毒可分为囊膜病毒和非囊膜病毒两大类。囊膜病毒的表面有糖蛋白、脂肪所形成的外膜。带有囊膜的病毒更容易进入宿主细胞,它帮助病毒在宿主体内扩散与繁殖,提高了病毒的致病性。
做“表面文章”的实验室当然不止高福一家。事实上,多年来科学家们潜心研究,已经发现了四种类型的病毒如何感染细胞的“表面文章”。
类型一以艾滋病毒为代表,它在细胞膜上,结合单个蛋白受体或辅助受体,实现与病毒的单个蛋白介导膜融合,也就是一把钥匙开一把锁,让病毒脱掉外膜与细胞融合。
类型二以疱疹病毒为代表,它在细胞膜上,结合多个受体或辅助受体,实现与病毒的多个蛋白介导膜融合,也就是多把钥匙开多把锁,让病毒脱掉外膜感染细胞。
类型三以流感病毒为代表,它在细胞膜上结合细胞膜表面受体后,并不急于融合,而是被细胞吞入内部后,形成内吞体,等内吞体内达到低pH值环境,再实现单个蛋白介导膜融合,也就是让病毒膜与内吞体膜融合,释放病毒遗传物质。
类型四以登革热病毒为代表,它不结合受体,直接内吞到细胞内吞体里,在低pH值环境里,实现单个蛋白介导膜融合。
而高福实验室解析出的埃博拉病毒的感染机制,与以上四种都不同。
扒开埃博拉的“迷彩服”
“我们在全世界第一个阐明埃博拉病毒与内吞体里的受体相互作用机制。”高福说,埃博拉病毒的特殊之处在于,以前发现的四类病毒,要么不结合特异性受体,要么在细胞膜上结合受体,而埃博拉不在细胞膜上结合受体,却在细胞内部,在内吞体膜上结合受体。
埃博拉病毒的入侵分为两步。
第一步是埃博拉病毒如何牢牢吸附在人体细胞表面。这一步的分子机制是高福团队率先发现的。他们发现,广泛分布于免疫细胞上的一种免疫分子——人TIM分子,不与埃博拉病毒囊膜表面糖蛋白直接相互作用,而是通过结合病毒囊膜上的磷脂酰丝氨酸分子PS来促进病毒感染,并阐明其结构基础。2015年12月,我国顶级中文科技期刊《科学通报》以封面文章发布了这一成果。
第二步是埃博拉病毒通过细胞内吞进入细胞内部,形成内吞体,在内吞体内,病毒发生膜融合过程,释放自身遗传物质。
此前,已有科学家研究发现内吞体膜上的NPC1分子是埃博拉病毒入侵所必须的,但是NPC1分子如何介导病毒入侵却一直是个未解之谜。
NPC1分子是负责胆固醇转运的多次跨膜蛋白,具有A、C、I三个大的腔内结构域。高福团队利用我国大科学装置“上海光源”对之解析发现,关键在C结构域。
埃博拉病毒囊膜表面糖蛋白在内吞体里经过宿主蛋白酶的酶切处理,变成激活态糖蛋白,暴露出受体结合位点,来与NPC1分子的C结构域发生相互作用,从而启动后续的病毒膜融合过程,实现病毒的感染生活史。
研究团队率先解析了NPC1分子的C区三维结构,发现它具有一个由α螺旋和β折叠组成的球状核心结构域,和两个突出来的环状结构。随后,研究人员解析出激活态糖蛋白与腔内结构域C的复合物三维结构,发现结构域C主要利用两个突出来的环状结构插入激活态糖蛋白头部的疏水凹槽里,从而发生相互作用。
这一重大发现预示着,人们能够针对激活态糖蛋白头部的疏水凹槽,去设计小分子或多肽抑制剂,来阻断埃博拉病毒的入侵过程。
进一步的分析发现,激活态糖蛋白与腔内结构域C结合后,会发生构象变化,使得糖蛋白的融合肽更容易暴露出来,插入内吞体膜上,从而启动膜融合过程。
高福解释说,NPC1是一把钥匙,而糖蛋白GP就是一把锁。当钥匙捅开了锁,埃博拉的感染过程就开始了。团队对NPC1的解析,扒开了埃博拉的“迷彩服”,弄清了钥匙的形状和位置,也弄清了钥匙开锁的整个过程。
这个重大发现写成论文后,高福团队于2015年10月底把它投递给美国的《细胞》杂志,12月23日杂志同意发表该文章。杂志编辑看出此发现的重要性,圣诞假期都不过了,加班加点弄出校正稿。“12月31日我就拿到校正稿,说是要在北京时间1月15日刊发。美国人民都急得不过圣诞假期了。”说起这篇论文受到的重视,高福很得意。
配一把堵锁眼的“钥匙”
走病毒的路,让病毒无路可走。
这就是新机制的发现出炉之后,高福团队的埃博拉特异性药物设计思路。
“如果你能模拟这个钥匙,未来就能开发出很多药物。”高福说,药物可以设计成钥匙的形状,在NPC1打开糖蛋白GP之前,就把锁眼堵上,让病毒无法在细胞内打开。
这类药物叫做竞争性抑制剂,公认的抗禽流感、甲型H1N1流感最有效药物之一的达菲,就属于竞争性抑制剂。
“我们会和国内其他实验室合作,尽快完成药物设计工作。”该篇论文的共同第一作者王寒、施一、宋健、齐建勋表示,实验室已有设计多肽和小分子药物的经验,目前正在跟国内其他科研单位合作,希望由中国人最先筛选出治疗埃博拉的特异性药物。
“2014年爆发的埃博拉疫情,现在已经平息了,但是我们和埃博拉的搏斗还没结束。”高福说,最新研究发现,埃博拉病毒可以在男性康复患者的精液中存活至少9个月。这种罕见的急性病毒长期携带案例,给科学家们提出了新课题,它预示着埃博拉随时可能死灰复燃,也意味着设计埃博拉特异性药物的意义重大。
根据过去的经验,在分子层面针对病原进行精准打击、直接作用于病毒的药物,既能断根治本,对人体的副作用也是最小的。现在,高福团队的发现,让人们有可能设计出这样的埃博拉治疗药物。
科学无国界,病毒泛滥也没有国界。
为了防控疫病的发生,高福团队多年来一直专注研究细胞表面,系统性地研究了包括H5N1、H7N9、甲型流感及新型蝙蝠流感在内的不同亚型流感病毒,及新型冠状病毒等多种囊膜病毒的蛋白与受体结合机制、病毒释放及病毒耐药机制,做出了一篇又一篇漂亮的“表面文章”,代表了这一领域研究的世界最高水平,发出了掷地有声、不容忽略的中国声音。
“这是长期积累的过程。中东呼吸综合征暴发时,我们也很快发表成果。”高福说,“我们对埃博拉的研究成果很多,就算再来个新病毒‘马博拉’也一样,只要是囊膜病毒,我们都可以解析,因为病毒研究平台已经建立”。
这个令人激动的新成果,也与我国这些年对基础研究加大投入有关。高福在采访中反复表示,如果没有上海光源,这个成果不可能最先在中国做出来。
“以前我们的口号是与国际接轨,但接轨就是接在尾巴上,跟在别人后面。中国现在已经成为世界GDP第二的大国,理应拥有一批世界领先的成果,这些都离不开科研基础设施和大科学装置的建设。”高福希望中国进一步加强科研基础设施建设,建立更多大科学装置和先进实验室,以推动更多更深入的科学基础研究。“我们的实践证明,基础科研也可以延伸到社会,服务于国民。”















 京公网安备 11010102002957号
京公网安备 11010102002957号